症例 70歳 女性 主訴:めまい
Profile:高血圧で近医にて内服治療中
現病歴:来院当日、回転性のめまいが出現し救急受診
頭位変換時にめまいが出現し、安静にしているとめまいはなし
脳神経異常は認めず
BPPV疑いで入院
血液検査にて低カリウム血症(K 2.8)あり
めまいで入院となったが、来院時の血液検査にて低K血症を認めた
高血圧で治療中であることから、原発性アルドステロン症が疑われ、スクリニーング検査施行
ARR>200であり、原発性アルドステロン症の疑いが濃厚となった
というように、原発性アルドステロン症はありふれています
原発性アルドステロン症
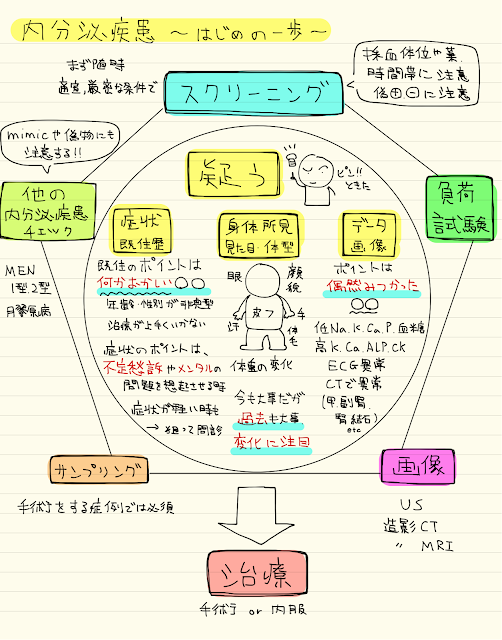
①まずは疑う:症状や既往歴、身体所見や見た目、血液検査や画像
②スクリーニング検査:閾値低く行う
③負荷試験:入院が必要になることが多い
④他の内分泌疾患や合併症のチェック:MENではないか、APSではないか
⑤画像検査:超音波検査、造影CT、MRI、シンチ
⑥サンプリング検査:専門施設で
⑦治療:手術 or 薬物治療
この7つの原則に沿って考えていきます
①疑う
症状としては、低カリウム血症の症状で脱力や筋力低下の症状があることがありますが、
症状はほとんどないことが多いです
既往歴・既存症としては、高血圧です
高血圧の10%は原発性アルドステロン症であると言われておりますので、
高血圧全例で原発性アルドステロン症を疑っても良いのですが、費用対効果は不明です
全例でスクリーニングをかけて検査するのは、労力や医療資源、時間の面で負担が大きいので、現実的ではない気がします
ですので、スクリーニングをかけるべき症例を見逃さないことが重要です
高血圧治療ガイドライン2019では、
低カリウム血症合併高血圧
若年者の高血圧
Ⅱ度(160/100以上)以上の高血圧
治療抵抗性の高血圧
副腎偶発腫を伴う高血圧
若年の脳血管障害合併を伴う高血圧
睡眠時無呼吸症候群を伴う高血圧
の際にスクリーニング検査が推奨されています
ポイントは何かがおかしい高血圧、つまり本態性と言い切れない高血圧の時に疑いましょう
②スクリーニング検査
血漿アルドステロン濃度(PAC)と血漿レニン活性(PRA)を測定し、
アルドステロン/レニン比(ARR)を計算します
ARR>200、PAC>120pg/mlで陽性と判断します
ただし検査の時間帯は午前中がよく、体位は30分の安静臥位、
薬は検査に影響を与える薬(ARBやACEは中止して2W後)は中止 など
条件が多いのが、スクリーニングのハードルをあげています
ですが、まずは難しいこと言わずに随時条件でもOKです
薬もMRA以外なら中止せず、そのまま検査してもOKです
随時条件や内服を継続したままスクリーニングを行って、
検査が陰性の場合に、薬剤変更を行ったり、条件を整えて検査することが実践的です
いろんな言い訳をして検査しないよりは、
まずは随時条件でもよいので、スクリーニング検査は実施すべきです
③負荷試験
いろいろありますし、国毎や学会によっても意見が異なります
ですが、1つでも陽性であれば、診断確定してよいのが、主流な考え方のようです
カプトプリル負荷試験が最も簡便で、外来でも可能です
原理
原発性アルドステロン症がなければ、
カプトプリル(ACE阻害薬)の服用により、アンギオテンシン1から2への変換が阻害され、
アンギオテンシン2が減少し、アルドステロン濃度(PAC)が低下します
その影響でレニンが上昇します(PRA)
そうするとARR(PAC /PRA)は低下します
原発性アルドステロン症では、アルドステロンの自律性分泌のため、
PACは低下せず、PRAも上昇しません
準備物:カプトプリル50mg
方法:早朝空腹状態で30分安静臥位にて負荷前採血(PAC、PRA)
カプトプリル50mgを内服
60分後、90分後に採血を行い、PACとPRAを測定する
判定基準:ARR>200で陽性
副作用:ほとんどなし
感度:66-100%、特異度:68-90%
他の検査
生理食塩水負荷試験:海外でよく行われている、特異度高い
方法:生理食塩水2Lを4時間で点滴後に採血
判定基準:PAC>60で陽性
副作用:心不全、高血圧
感度:83%、特異度:75-100%
フロセミド立位負荷試験
方法:フロセミド40mgを静注し、2時間立位保持後に採血
判定基準:PRA<2.0
副作用:血圧低下、転倒、意識消失
感度:?、特異度:?
まずはカプトリル負荷試験を考慮
症例に応じて、生理食塩水負荷試験やフロセミド立位負荷を追加する
④他の内分泌疾患や合併症のチェック
SASの合併やAf、心不全、strokeの合併が多いので注意が必要です
スクリーニング検査で原発性Ald症らしくなければ、
腎血管性などの二次性高血圧の鑑別が必要な時もあります
⑤画像検査
副腎造影CT検査を行います
褐色細胞腫が否定できない場合はまずは単純CTを行います
5mm以下のmicroadenomaの腺腫は検出できません
腺腫が確認された場合は、
他のホルモン(コルチゾール、ACTH、DHEAーS、尿中カテコラミン分画、メタネフリン分画)のチェックも必要です
また年単位での経過観察も必要になります
年間1cm以上の増大を認める場合や4cm以上(特に6cm以上)の場合は、
副腎がんや悪性腫瘍の転移の可能性もあり、注意が必要です
⑥サンプリング
手術してよいか、手術してはいけないかを決める重要な検査です
画像で明らかに腺腫が確認されても、両側性の場合がありますので、
必ず副腎静脈サンプリング(AVS)が必要です
サンプリング時に
⑦治療
原発性アルドステロン症で大事なのは、ゴールの設定だと思っています
片側性の腺腫の場合、現代医学の推奨されるゴールは手術です
ですが、原発性アルドステロン症の患者さんの多くは、困っていませんので、
患者さんが手術を望まれない時も往々にしてあります
重要なのは、原発性アルドステロン症という病気や治療について、
患者さんにもしっかり理解してもらい、一緒に治療方針を決めていくことです
手術してもMRA(ミネラルコルチコイド受容体拮抗薬)の薬で管理しても、
予後に差はありませんが、
手術のメリットとしては、内服治療しなくてよくなる点です
手術のデメリットとしては、労力(時間、お金)、体への負担です
患者さんが困っていないことや内服でも予後に差がないので、
積極的に手術に進む症例は限られているのが現状だと思っています
原発性アルドステロン症で手術を希望されない方は、
MRAで血圧コントロールやKのコントロールを行います
手術せず、MRAで治療されている方も多いので、MRAに精通しておくことが重要です

0 件のコメント:
コメントを投稿